Lysosomes
« It is obvious that no great advance can be made in the study of cell structure unless we succeed in separating the various cell constituents and obtain them in quantities sufficient to permit the application of the usual analytical methods.
Albert Claude (1941)
Glucose 6-phosphatase
L’insuline est une hormone secrétée par les cellules β des îlots de Langherans du pancréas ; elle participe au maintien dans des limites étroites de la concentration sanguine en glucose : lorsque la glycémie augmente au-delà d’une limite supérieure, le pancréas déverse de l’insuline dans le courant sanguin. L’hormone se fixe sur un récepteur de la surface des cellules hépatiques ; celles-ci captent des molécules de glucose dans la circulation sanguine et les stockent sous forme de glycogène, un polymère de glucose qui s’accumule en « rosettes » dans le cytosol des hépatocytes. Lorsque l’organisme a besoin d’énergie, des molécules de glucose sont détachées du glycogène et la glycogène phosphorylase transforme le glucose en glucose 1-phosphate puis en glucose 6-phosphate. La glucose 6-phosphatase hydrolyse cet ester phosphate et libère du glucose qui passe dans la circulation sanguine :
Glucose 6-phosphate + H2O → Glucose + Pi
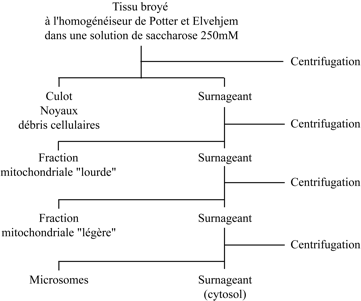
L’existence de cet enzyme fut découverte par Gerty T. Cori, Carl F. Cori et Gerhard Schmidt G (Department of Pharmacology, Washington University School of Medicine, St Louis). Henri Géry Hers (Laboratoire de chimie physiologique, Université Catholique de Louvain) entreprit sa purification à partir de foie de rat ; après précipitation à pH 5, il était impossible de remettre l’enzyme en solution. Dans son article de 1946, dans The Journal of Experimental Medicine, Albert Claude (Rockefeller Institute for Medical Research) insistait sur le fait que les organites subcellulaires s’agglutinent de manière irréversible à pH 5 ; il se forme des agrégats si le milieu utilisé pour homogénéiser les tissus n’est pas ajusté à un pH voisin de la neutralité. Christian de Duve en déduisit que la glucose 6-phosphatase est associée à un organite subcellulaire. La façon de le vérifier était de recourir au fractionnement subcellulaire. Jacques Berthet adapta la technique de Claude au fractionnement d’un homogénat de foie de rat, en prenant en compte les améliorations apportées par George Hogeboom, Walter Schneider et George Palade (Rockefeller Institute for Medical Research) : homogénéisation des tissus avec l’appareil en verre et piston en téflon de Potter et Elvejhem (Claude utilisait un mortier et un pilon) dans une solution de saccharose 250 millimolaire (Claude utilisait des solutions salines). Le protocole aboutissait à la séparation de trois fractions particulaires : fraction nucléaire, gros granules (Large Granules), petits granules (Small Granules) et d’un surnageant. La glucose-6 phosphatase sédimentait principalement dans la fraction des petits granules (microsomes), mais les fractions nucléaires et des gros granules (fraction mitochondriale) en contenaient aussi.
Références : Cori GT, Cori CF, Schmidt G The role of glucose-1-phosphate (1939)
Claude A Fractionation of mammalian liver cells by differential centrifugation (1946)
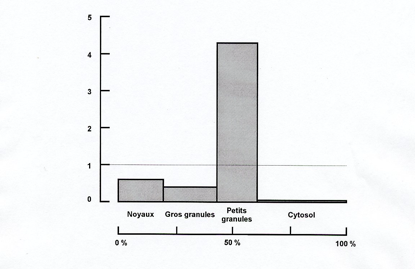 |
| La glucose 6-phosphatase est présente en proportions variables dans toutes les fractions particulaires. Ordonnée : activité spécifique relative ; abscisse : teneur en protéine (en % de l’homogénat) |
Ce résultat pouvait être interprété de deux façons : (i) les organites ont une composition enzymatique hétérogène ; il y a de la glucose 6-phosphatase en proportions variables dans les noyaux, les mitochondries et les microsomes, ceux-ci étant les plus riches en phosphatase ; (ii) les fractions subcellulaires sont hétérogènes ; la glucose 6-phosphatase n’est présente que dans les microsomes ; sa présence dans les fractions nucléaire et mitochondriale s’explique par l’existence d’une contamination par des microsomes. Il était logique de supposer que, pour qu’un organite remplisse une ou des fonctions spécifiques au sein de la cellule, il doit disposer d’un équipement enzymatique spécifique. Christian de Duve et Jacques Berthet optèrent pour cette interprétation et, à l’époque, ils furent parmi les premiers sinon les seuls à le faire. Le postulat de la localisation unique (un enzyme n’est présent que dans un seul type d’organite) allait jouer un rôle essentiel dans l’interprétation des résultats du fractionnement subcellulaire.
Ce point mérite qu’on s’y attarde. Dans une population d’organites comme celle des mitochondries, par exemple, les tailles varient : il y a de grosses mitochondries, des petites et, entre les deux, un éventail de mitochondries de taille moyenne. Il en va de même pour les lysosomes, dont la taille est en moyenne voisine de celle des mitochondries. Les populations d’organites sont « polydisperses ». La taille d’un organite déterminant sa vitesse de sédimentation, les fractions isolées sont des mélanges en proportions variables d’organites de taille semblable, mais appartenant à des populations différentes, ce qui se traduit sur le plan biochimique par le fait que « les fractions contiennent un peu de tout ». De nombreux expérimentateurs commirent l’erreur de conclure que les enzymes de la fraction mitochondriale étaient tous présents dans les mitochondries. Au début des années 1950, la confusion entre fraction et organite conduisit des biochimistes à conclure que les chloroplastes contiennent de la peroxydase (un enzyme des peroxysomes). L’interprétation correcte du résultat de l’expérience représentée dans la figure ci-dessus est donc que la glucose 6-phosphatase est un enzyme microsomial et que les fractions nucléaire et mitochondriale sont contaminées par des microsomes en proportions variables. Les aspects théorique et pratique du fractionnement subcellulaire par centrifugation différentielle furent exposés dans l’article publié en 1954 par de Duve et Berthet dans International Review of Cytology.
Référence : De Duve C, Berthet J The use of differential centrifugation in the study of tissue enzymes (1954)
Phosphatase acide
La glucose-6 phosphatase fut le premier enzyme identifié dans les microsomes à une époque où le lien entre microsomes et réticulum endoplasmique n’était pas encore établi avec certitude. Sa distribution dans les fractions fut comparée à celle de la phosphatase acide, un enzyme hydrolysant aussi le glucose 6-phosphate, mais à une vitesse moins élevée que la glucose-6 phosphatase. Pour le dosage de la phosphatase acide, le substrat utilisé était une molécule synthétique : le β-glycérophosphate. Nous savons aujourd’hui que le substrat in vivo de la phosphatase acide est un sucre phosphorylé : le mannose 6-phosphate. Les enzymes destinés aux lysosomes sont des glycoprotéines synthétisées dans le reticulum endoplasmique. Elles portent une chaîne glycanique se terminant par un mannose. Dans le cis-Golgi, ce mannose est phosphorylé. Dans le trans-Golgi, l’enzyme portant l’« étiquette mannose 6-phosphate » est reconnu par un récepteur spécifique. Les enzymes liés au récepteur sont séquestrés dans des vésicules qui se détachent du trans-Golgi et s’acidifient progressivement par fusion avec des endosomes. Au pH lysosomial (4,8), le mannose 6-phosphate se détache du récepteur et les enzymes lysosomiaux sont libérés. Le rôle de la phosphatase acide est d’hydrolyser la liaison ester phosphate du mannose 6-phosphate. La chaîne glycanique des glycoprotéines lysosomiales ne porte pas de mannose 6-phosphate.
Après fractionnement par centrifugation d’un homogénat de foie de rat, la phosphatase acide présentait une particularité : dans les fractions fraîchement préparées, son activité était faible ; dans les fractions conservées quelques jours au réfrigérateur, elle était dix fois plus élevée. Une partie de l’activité dans les fractions « fraîches » était masquée – phénomène qualifié de « latence enzymatique ». Les traitements altérant les membranes (vieillissement, congélation et décongélation, traitement mécanique, détergents) démasquaient l’activité. Christian de Duve formula l’hypothèse que la phosphatase acide était localisée à l’intérieur d’un organite entouré d’une membrane imperméable au substrat (β-glycérophosphate) et que l’imperméabilité de cette membrane était abolie par le vieillissement des fractions. Cet organite hypothétique semblait distinct des mitochondries, sans que l’on puisse exclure qu’il s’agisse de petites mitochondries, de mitochondries « légères » ou de fragments de mitochondries [1], [2] . Deux autres enzymes se comportaient comme la phosphatase acide (sédimentation dans la fraction mitochondriale, maximum d’activité à pH 5, phénomène de latence) : la β-glucuronidase (qui hydrolyse les esters d’acide glucuronique) et la cathepsine (une protéase).
Références : Berthet J, de Duve C Tissue Fractionation Studies. I. The existence of a mitochondria-linked, enzymatically inactive form of acid phosphatase in rat-liver tissues (1951)
de Duve C, Berthet J, Berthet L, Appelmans F Permeability of Mitochondria (1951)
A la suite d’une modification du protocole de fractionnement, la fraction des gros granules fut séparée en deux fractions appelées respectivement M (Mitochondria) et L (Light Mitochondria). Avec le schéma de fractionnement de Claude, la cytochrome oxydase sédimentait pour l’essentiel dans la fraction mitochondriale, la glucose 6-phosphatase dans les microsomes et la phosphatase acide occupait une position intermédiaire entre cytochrome oxydase et glucose 6-phosphatase. Après modification, le profil de distribution de la phosphatase acide changea radicalement : il présentait un pic dans la fraction L et se démarquait nettement des distributions de la cytochrome oxydase et de la glucose 6-phosphatase. L’hypothèse d’une association de la phosphatase acide à de petites mitochondries perdait de sa crédibilité ; on était plutôt en présence d’un organite de nature inconnue. En parcourant la littérature scientifique, Jacques Berthet dressa une liste d’enzymes présentant une distribution intermédiaire entre mitochondries et microsomes. Leur distribution dans les fractions N (Nuclei), M (Mitochondria), L (Light mitochondria), P (Particles), S (Supernatant) fut comparée à celle de la phosphatase acide. Deux nucléases montraient des profils de distribution et une latence comparables à ceux de la phosphatase acide, de la β-glucuronidase et de la cathepsine D. Ces enzymes étaient aussi des hydrolases. Le concept d’organite lytique ou lysosome prit naissance en 1955. Aux critères enzymatiques et physicochimiques, il fallait ajouter des critères morphologiques, c’est-à-dire « voir » les organites lytiques dans la cellule.
Voir les lysosomes
Dans un article publié en 1953 dans The Journal of Histochemistry and Cytochemistry, Alex B. Novikoff (Albert Einstein College of Medicine) décrivait les résultats d’expériences de fractionnement subcellulaire : dans les cinq fractions particulaires isolées : nucléaire, mitochondriale, mixte, microsomiale I, microsomiale II, et dans le surnageant, il a dosé une série de constituants chimiques et enzymatiques choisis avec une remarquable pertinence car ils seront plus tard universellement utilisés comme « marqueurs » des principaux organites : ADN (noyaux), ARN (noyaux, reticulum endoplasmique rugueux, surnageant), succinate oxydase (mitochondries), phosphatase acide (lysosomes), uricase (peroxysomes), estérase (reticulum endoplasmique), phosphatase alcaline et 5’-nucléotidase (membrane plasmique). Les distributions dans les fractions se recouvraient largement les unes les autres et Novikoff en tira la conclusion que la composition biochimique des organites était hétérogène.
Rétrospectivement, il peut paraître surprenant que tant de biochimistes aient opté pour le postulat d’hétérogénéité ; ce postulat peut s’interpréter de deux façons : (i) les organites sont biochimiquement hétérogènes ; il y a « de tout partout » ; (ii) la composition d’un type d’organite (les mitochondries, par exemple) est hétérogène ; il y a des mitochondries avec beaucoup de succinate oxydase et d’autres qui en contiennent peu. La première hypothèse semble peu logique. Elle reviendrait à dire qu’un organite donné n’exerce pas de fonction spécifique dans la cellule, qu’il n’y a pas de relation entre structure et fonction.
Alex Novikoff comprit la portée de la découverte du Groupe de Louvain et accéda à la demande de Christian de Duve de collaborer à l’identification des lysosomes au microscope. Il profita de la tenue à Bruxelles du Third International Congress of Biochemistry, en 1955, pour faire un séjour dans le Laboratoire de Chimie physiologique, à Louvain. Henri Beaufay prépara des fractions enrichies en phosphatase acide (fraction L). Le laboratoire ne possédant pas de microscope électronique, Novikoff utilisa celui d’Albert Claude à l’Institut Bordet, à Bruxelles. Le contact entre les deux microscopistes ayant produit d’importantes décharges électriques, Novikoff effectua un repli stratégique vers l’Institut de Recherches sur le Cancer du Centre National de la Recherche Scientifique, à Villejuif, où il bénéficia de l’hospitalité de Wilhelm Bernhard. L’article publié en 1956 contenait une micrographie de la fraction L (light) montrant des vésicules au contenu hétérogène, de différentes tailles, entourées d’une membrane simple ; il contenait aussi une micrographie de Wilhelm Bernhard et Charles Rouiller montrant des vésicules semblables dans le cytoplasme d’hépatocyte de rat. Rouiller avait découvert ces organites en 1954 et, ignorant leur fonction dans la cellule, les avait baptisés « corps denses péri-canaliculaires » par référence à leur localisation préférentielle à proximité des canaux biliaires.
En 1961, Novikoff adapta à la microscopie électronique la technique de Gyorgy Gömöri (University of Chicago) pour révéler la présence de phosphatases dans les tissus. Le principe en était simple : l’hydrolyse du β-glycérophosphate libère du phosphate qui est capturé sous forme de sel de plomb, opaque aux électrons ; la transformation du phosphate de plomb en sulfure de plomb confère aux lysosomes une coloration brun foncé. La cellule renferme de nombreuses phosphatases ; pour éviter leur interférence dans la réaction cytochimique, le pH du milieu d’incubation est ajusté au pH optimum d’activité de la phosphatase acide (4,5). Les lysosomes purent ainsi être identifiés dans toutes les cellules eucaryotes (sauf les globules rouges), parfois jusqu’à plusieurs centaines par cellule. Ils présentent une grande hétérogénéité de taille, de forme et de contenu et sont entourés d’une membrane. A cause de leur caractère hétérogène (polydisperse, en jargon de physico-chimiste) il est difficile d’isoler par centrifugation une fraction de lysosomes dépourvue de contaminants, d’autant que les lysosomes sont des composants « mineurs » de la cellule (environ 1% des protéines cellulaires).
Références : Novikoff AB Biochemical heterogeneity of the cytoplasmic particles isolated from rat liver homogenates (1953)
Alex B. Novikoff AB, Henri Beaufay H, Christian de Duve C, Electron Microscopy of Lysosome-rich Fractions from Rat Liver, Journal of Biophysical and Biochemical Cytology (1956)
Gomori G Microtechnical demonstration of phosphatase in tissue sections (1939)
Gomori G Alkaline phosphatase of cell nuclei (1951)
L’appareil cellulaire de dégradation des macromolécules
Les lysosomes sont des organites de 0,2 à 0,5 micromètre, responsables de la dégradation des macromolécules de la cellule et du recyclage des produits de cette dégradation. Pour remplir cette fonction de digestion, intra- ou extra-cellulaire chez les ostéoclastes, chondroblastes et macrophages, ils disposent d’un équipement enzymatique très complet leur permettant d’hydrolyser les acides nucléiques, les protéines et les hydrates de carbone complexes. Le matériel à digérer parvient aux lysosomes par trois voies : (i) l’endocytose, avec passage du matériel par les endosomes ; (ii) la phagocytose d’organites subcellulaires endommagés, avec formation d’un autophagosome et fusion avec un lysosome ; ce mécanisme est appelé : autophagie ; (iii) la phagocytose dans les leucocytes, avec formation d’une vésicule contenant une bactérie, un parasite ou du matériel à dégrader ; la vésicule fusionne avec un lysosome.
Les lysosomes sont limités par une bicouche phospholipidique unique issue du complexe de Golgi ; sa composition en phospholipides se caractérise par une concentration élevée en sphingomyéline et cholestérol, ce qui lui confère stabilité et résistance. La membrane contient également de l’acide lyso-bis-phosphatidique (bis-mono-acyl glycérol-phosphate), surtout celle des endosomes tardifs (15 à 20% de leurs phospholipides).
La membrane des lysosomes contient environ 25 protéines intégrales dont la moitié sont des glycoprotéines. Les plus abondantes sont les protéines LAMPs 1, 2, (Lysosome Associated Membrane Proteins), LIMPs 1, 2 (Lysosome Integral Membrane Proteins) et CD63, une glycoprotéine de la famille des tétraspanines, impliquées, entre autres fonctions, dans l’adhésion cellulaire. Les LAMPs ont un court domaine cytoplasmique, suivi d’une séquence d’insertion transmembranaire ; le domaine luminal est hyper glycosylé : les chaînes oligosaccharidiques liées à des asparagines contribuent pour plus de la moitié (60 %) du poids moléculaire (90 à 120 kDa) ; elles forment sur la face interne de la membrane un glycocalyx qui la protège contre l’autodigestion par les lipases et les protéases. R. Kundra et Stuart Kornfeld (Washington University School of Medicine, Division of Hematology, St. Louis) ont montré que si l’on retire leurs chaînes glycaniques par un traitement à l’endoglycosidase H, LAMP 1 et LAMP 2 sont rapidement dégradées.
Références : Kundra R, Kornfeld S Asparagine-linked oligosaccharides protect Lamp-1 and Lamp-2 from intracellular proteolysis (1999)
Schoer JK, Gallegos AM, McIntosh AL, Starodub O, Kier AB, Billheimer JT, Schroeder F Lysosomal Membrane Cholesterol Dynamics (2000)
Goder V, Spiess M Topogenesis of membrane proteins: determinants and dynamics (2001)
La protéine LAMP 1 est utilisée comme marqueur de sénescence des cellules, et de différenciation des cellules des métastases tumorales – elle faciliterait l’adhésion et la migration des cellules tumorales.
Référence : Meca-Laguna G, Qiu M, Hou Y, Barkovskaya A, Shankar A, Dixit B, Rae MJ, Boominathan A, Sharma A Cell-Surface LAMP1 is a Senescence Marker in Aging and Idiopathic Pulmonary Fibrosis (2025)
LIMP-1 (35 à 55 kDa) et LIMP-2 (LGP 85) sont des glycoprotéines insérées dans la membrane par une séquence signal NH2-terminale non clivable et par un court domaine C-terminal ; elles ont plusieurs domaines trans-membranaires : deux à quatre pour LIMP-1, deux pour LIMP-2. Ces protéines sont des récepteurs actifs dans le transport d’enzymes ; c’est ainsi que LIMP-2 joue un rôle essentiel dans le transfert de la β-glucocérébrosidase dans les lysosomes. Cette hydrolase acide catalyse la réaction :
glucocérébroside → glucose + céramide
et plus généralement le catabolisme des glycosphingolipides. Dans la maladie de Gaucher et le syndrome myoclonie-insuffisance rénale, la déficience en β-glucocérébrosidase se traduit par une accumulation de lipides dans les macrophages. LIMP-2 est un récepteur actif dans le transport des lipides ; elle s’associe à une protéine membranaire des endosomes tardifs : STARD3 (StAR-related lipid transfer Domain-3), pour transporter le cholestérol exogène vers la membrane lysosomale et les gouttelettes lipidiques, des organites de stockage des triglycérides et des esters de stérols. STARD3 établit des contacts avec la protéine VAPB (VAMP-Associated Protein B), une protéine membranaire du reticulum endoplasmique. Les sites de contact établis avec les lysosomes servent de lieux d’échanges de matériel. LIMP-2 est une protéine hyper-glycosylée, traversée par une cavité hydrophobe par laquelle transitent les lipides. Elle joue un rôle dans la biogenèse et l’homéostasie des lysosomes, ainsi que dans la régulation de l’autophagie, en stimulant la maturation d’auto-phagosomes.
Références : Schneede A, Schmidt CK, Höltta-Vuori M, Heeren J, Willenborg M, Blanz J, Domanskyy M, Breiten B, Brodesser S, Landgrebe J, Sandhoff K, Ikonen E, Saftig P, Eskelinen EL Role for LAMP-2 in endosomal cholesterol transport (2011)
Li J, Pfeffer SR Lysosomal membrane glycoproteins bind cholesterol and contribute to lysosomal cholesterol export (2016)
Heybrock S, Kanerva K, Meng Y, Ing C, Liang A, Xiong ZJ, Weng X, Kim YA, Collins R, Trimble W, Pomès R, Privé GG, Annaert W, Schwake M, Heeren J, Lüllmann-Rauch R, Grinstein S, Ikonen E, Saftig P, Neculai D Lysosomal integral membrane protein-2 (LIMP-2/SCARB2) is involved in lysosomal cholesterol export (2019)
LIMP-2 jouerait aussi un rôle dans la régulation du compartiment endolysosomal, en interagissant avec la machinerie moléculaire de fusion et fission vésiculaires. Toshio Kuronita et coll. (Division of Pharmaceutical Cell Biology, Graduate School of Pharmaceutical Sciences, Kyushu University, Fukuoka) ont mis en évidence son rôle dans la biogenèse, et l’organisation spatiale du compartiment endosomes/lysosomes.
Référence : Kuronita T, Eskelinen EL, Fujita H, Saftig P, Himeno M, Tanaka Y A role for the lysosomal membrane protein LGP85 in the biogenesis and maintenance of endosomal and lysosomal morphology (2002)
La membrane des lysosomes renferme des perméases, une pompe à protons électrogène (pompe à protons vacuolaire, H+-ATPase de type V) utilisant l’énergie libérée par l’hydrolyse de l’ATP, et des canaux ioniques aux ions chlorures Cl−. Ces constituants participent au maintien du pH intra-lysosomal entre 5,2 et 5,5, le pH optimal d’activité des hydrolases acides ; ils participent aussi à l’importation de matériaux et à l’exportation de métabolites.
La membrane des lysosomes renferme des transporteurs actifs entre le compartiment lysosomal et le cytosol : (i) le Transporteur membranaire d’acides aminés cationiques PQLC2 (PQ Loop repeat-Containing protein 2) exporte les acides aminés Arginine, Histidine, Lysine et régule l’homéostasie des acides aminés cationiques ; (ii) la Cystinosine, un co-transporteur (symport) cystine – H+, exporte la cystine, un produit de dégradation des protéines par les protéases lysosomales ; la cystine est formée de deux molécules de cystéine, un acide aminé portant un groupe sulfhydryle. Le Transporteur d’acides aminés cationiques PQLC2 et la cystinosine appartiennent à la famille des protéines à sept hélices transmembranaires, comme la bactériorhodopsine, la pompe à protons des Archées. Leur structure tridimensionnelle se caractérise par deux boucles PQ (PQ loop), un motif conservé chez les protéines impliquées dans le changement du potentiel de membrane par transfert de charges électriques (transport électrogénique) et l’homéostasie des acides aminés cationiques. (iii) Le Transporteur d’acide sialique (sialine) transporte ce sucre acide libéré lors de la dégradation des glycoprotéines, des glycosaminoglycanes et des glycolipides (Havelaar et al., 1999) ; (iv) Il existerait aussi un transporteur de glucose dans les lysosomes de foie de rat.
Références : Kalatzis V, Cherqui S, Antignac C, Gasnier B Cystinosin, the protein defective in cystinosis, is a H(+)-driven lysosomal cystine transporter (2001)
Jézégou A, Llinares E, Anne C, Kieffer-Jaquinod S, O’Regan S, Aupetit J, Chabli A, Sagné C, Debacker C, Chadefaux-Vekemans B, Journet A, André B, Gasnier B Heptahelical protein PQLC2 is a lysosomal cationic amino acid exporter underlying the action of cysteamine in cystinosis therapy (2012)
Talaia G, Amick J, Ferguson SM Receptor-like role for PQLC2 amino acid transporter in the lysosomal sensing of cationic amino acids (2021)
Mancini GM, de Jonge HR, Galjaard H, Verheijen FW Characterization of a proton-driven carrier for sialic acid in the lysosomal membrane: Evidence for a group-specific transport system for acidic monosaccharides (1989)
Mancini GM, Beerens CE, Verheijen FW Glucose transport in lysosomal membrane vesicles. Kinetic demonstration of a carrier for neutral hexoses (1990)
Les lysosomes sont au cœur du système digestif de toutes les cellules, à l’exception des globules rouges. Pour dégrader les acides nucléiques, les protéines, les polysaccharides, les phospholipides, les sphingolipides, les glycoconjugués, ils disposent d’un arsenal d’une cinquantaine d’hydrolases : protéases, peptidases, nucléases, glycosidases, lipases, phospholipases, sulfatases, qui exercent leur fonction en milieu acide (qui dénature les protéines et les complexes protéiques et facilite ainsi leur digestion).
La protéine LBP-8 (Fatty Acid-Binding Protein homolog 8) est une chaperone qui transfert des acides gras insaturés dans le noyau ; elle appartient à la famille des protéines intracellulaires fixant les lipides (iLBP, Lipid-Binding Protein 8) ; elle est impliquée dans la voie de signalisation rétrograde entre lysosomes et noyau (lysosome to-nucleus retrograde signaling pathway), dans laquelle elle participe à l’activation de gènes de longévité.
Les lysosomes constituent le principal compartiment acide de la cellule. Pour mesurer leur pH interne, on a utilisé des macromolécules colloïdales ou des liposomes portant une sonde fluorescente sensible à la concentration en protons du milieu ; le complexe parvenait aux lysosomes par la voie endocytaire. Les valeurs de pH rapportées dans la littérature oscillaient entre 3,5 et 5,5 pour les lysosomes et entre 4,6 et 6,2 pour les endosomes. La faiblesse de cette approche est la dépendance de la mesure à la quantité de complexe introduite dans l’organite. Ce biais expérimental a été corrigé en utilisant du dextran auquel on a couplé deux sondes fluorescentes, l’une sensible au pH – l’isothiocyanate de Fluorescéine -, l’autre insensible au pH – la Rhodamine. La valeur du pH est déduite du rapport entre l’intensité de la fluorescence émise par les deux signaux (mesurée par spectroscopie) ; elle est indépendante de la concentration de la sonde fluorescente que l’on est parvenu à introduire dans l’organite. On a aussi utilisé des variantes de la Protéine verte fluorescente (Green Fluorescent Protein) sensibles à la concentration du milieu en protons ; pour cibler les lysosomes, on l’a fusionnée à la protéine membranaire LAMP1.
Référence : Ohkuma S, Poole B Fluorescence probe measurement of the intralysosomal pH in living cells and the perturbation of pH by various agents (1978)
Les mesures les plus précises sont obtenues en utilisant une nanomachine à ADN sensible à des stimuli extérieurs en changeant de conformation moléculaire. La nanomachine I-switch, mise au point par Souvik Modi et coll. (National Centre for Biological Sciences, Tata Institute of Fundamental Research, Bangalore), est sensible à la concentration en protons du milieu ; c’est un « senseur » de l’acidité du milieu (pH), basé sur la capture du transfert d’énergie de résonance (Förster Resonance Energy Transfer, FRET) d’une molécule « donneuse » excitée. Un ADN bicaténaire est synthétisé par ingénierie moléculaire ; les deux brins sont riches en cytosine, une base pyrimidique avec un groupe amine en position C4. À pH neutre, la structure nucléotidique est « ouverte ». Placée dans un environnement acide, les cytosines fixent des protons et s’intercalent provoquant le repliement de la structure moléculaire qui se referme sur elle-même (I-motif switch) ; ce changement de conformation rapproche deux molécules fluorescentes créant un signal (FRET), dont la mesure donne la valeur du pH.
Référence : Modi S, Swetha MG, Goswami D, Gupta GD, Mayor S, Krishnan Y A DNA nanomachine that maps spatial and temporal pH changes inside living cells (2009)
Revue générale : Mindell JA Lysosomal acidification: mechanisms and diseases (2012)
Les matériaux à digérer venant de l’extérieur parviennent aux lysosomes par l’intermédiaire des endosomes. On a mis en évidence l’existence d’une voie endocytaire « acide » qui prend naissance avec les vésicules d’endocytose, à partir d’invaginations de la membrane plasmique, passe par les endosomes précoces (pH 6,2 à 6,5), les endosomes tardifs (pH 5,0 à 5,5) et aboutit aux lysosomes (pH 4,5 à 5,0). Ce processus graduel d’acidification facilite la dénaturation et la dégradation par les hydrolases acides des ligands internalisés par la cellule. La fonction digestive est assurée par une impressionnante panoplie d’hydrolases : glycosidases (40), protéases (18), sulfatases (7), nucléases, lipases, phospholipases, phosphatases, et les activateurs de dégradation des sphingolipides (Sphingo Activator PrO(S)teIN) : les saposines. Les macromolécules sont internalisées dans les cellules par endocytose « médiée » par récepteur. C’est le cas pour les lipoprotéines de faible densité circulant dans le sang, comme le montrèrent Richard G. Anderson, Michael S. Brown et Joseph L. Goldstein (University of Texas) ; ces deux derniers se virent attribuer le prix Nobel de médecine ou physiologie 1985. Les lipoprotéines, chargées de cholestérol, sont reconnues par un récepteur spécifique de la surface cellulaire. Un mécanisme similaire a été décrit pour la transferrine, une β-globuline qui transporte deux atomes de fer par molécule, de l’intestin vers le foie ou les réticulocytes. L’internalisation de la globuline et des atomes de fer complexés met en œuvre le récepteur de la transferrine de la membrane plasmique.
Références : Brown MS, Goldstein JL Familial hypercholesterolemia: Defective binding of lipoproteins to cultured fibroblasts associated with impaired regulation of 3-hydroxy-3-methylglutaryl coenzyme A reductase activity (1974)
Brown MS, Goldstein JL Analysis of a mutant strain of human fibroblasts with a defect in the internalization of receptor-bound low density lipoprotein (1976)
Anderson RG, Goldstein JL, Brown MS A mutation that impairs the ability of lipoprotein receptors to localise in coated pits on the cell surface of human fibroblasts (1977)
Gilbert Ashwell et Anatol G. Morell (National Institute of Arthritis, Metabolism, and Digestive Diseases) montrèrent en 1968 que c’est également le cas pour la céruléoplasmine, une glycoprotéine de la circulation sanguine. La perte de l’acide sialique périphérique expose les résidus galactose de la chaîne glycanique ; ils sont reconnus par un récepteur de la membrane plasmique des hépatocytes, identifié par Ashwell et la céruléoplasmine est internalisée dans la cellule. Ce sont les résultats d’Ashwell et Morell qui ont révélé l’existence de l’endocytose des glycoprotéines circulantes médiée par un récepteur (Asialoglycoprotein receptor mechanism).
Article de revue : Ashwell G, Morell AG The role of surface carbohydrates in the hepatic recognition and transport of circulating glycoproteins (1974)
L’internalisation des macromolécules reconnues par les récepteurs de la membrane péricellulaire commence avec l’invagination de celle-ci au niveau des puits tapissés de molécules de clathrine. L’invagination s’accentue jusqu’à la formation d’une vésicule tapissée de clathrine formant un squelette (une « cage »). Les puits tapissés de clathrine furent observés au microscope électronique par Thomas Roth et Keith Porter en 1964 et isolés par Barbara M.F. Pearce (Laboratory of Molecular Biology, Medical Research Council, Cambridge) en 1975 à partir de tissus nerveux où ces organites sont abondants. En 1976, elle en purifia le principal constituant protéique, la clathrine, une protéine formée de trois branches (triskélion) ayant la propriété de s’assembler en une structure en forme de polyèdre. Le matériel endocyté dans les vésicules est dirigé vers les endosomes primaires où ils sont rejoints par les hydrolases acides synthétisées dans le reticulum endoplasmique et ayant transité par le trans-Golgi. Les endosomes primaires deviennent des endosomes secondaires ou des lysosomes. Les liquides, contenant généralement des substances dissoutes ou des substances adsorbées sur la membrane plasmique, sont intériorisés dans la cellule par un mécanisme particulier d’endocytose non spécifique appelé pinocytose.
Références : Roth TF, Porter KR Yolk protein uptake in the oocyte of the mosquito Aedes aegypti (1964)
Pearse BMF Clathrin: a unique protein associated with intracellular transfer of membrane by coated vesicles (1976)
Chez certaines cellules spécialisées, les lysosomes sont alimentés en matériaux à digérer par la phagocytose, une forme d’hétérophagie active. Elle fut observée pour la première fois en 1882 chez les larves mobiles d’étoile de mer par le zoologiste Ilya (Elie) Metchnikov (prix Nobel de médecine ou physiologie 1908). Après avoir inséré des épines de rosier dans ces larves, il observa que des cellules mobiles s’étaient rassemblées pour « manger » (phagein en grec) ces corps étrangers.
Référence : Metchnikov E Untersuchungen über die mesodermalen Phagocyten einiger Wirbeltiere (1883)
Le sang circulant renferme des phagocytes « professionnels », les macrophages et les leucocytes neutrophiles, aussi appelés « polymorphonucléaires » par référence à la forme multilobée de leur noyau. Ces cellules jouent un rôle actif dans la défense de l’organisme : elles possèdent la capacité de capturer des bactéries ou des débris cellulaires dans le milieu extérieur en les englobant dans un repli de leur membrane plasmique, et de les internaliser dans une vésicule entourée d’une membrane : le phagosome. Cet organite se déplace sur les microfilaments d’actine du cytosquelette de la cellule pour aller fusionner avec les endosomes puis avec les lysosomes ; on a désigné ce phénomène : « flux de membrane endolytique ». Les pompes à protons abaissent le pH du phagolysosome jusqu’à une valeur comprise entre 4,5 et 5,0. Les hydrolases lysosomiales entrent alors en action pour digérer le contenu. Les produits d’hydrolyse sont exportés dans le cytoplasme pour être recyclés. Les résidus non-digestibles, s’il y en a, s’accumulent en un corps résiduel qui peut être éliminé par exocytose. Chez les amibes, la phagocytose est très active ; elle joue le rôle de mécanisme nutritionnel plutôt que de mécanisme de défense.
Article de revue : Levin R, Grinstein S, Canton J The life cycle of phagosomes: formation, maturation, and resolution (2016)
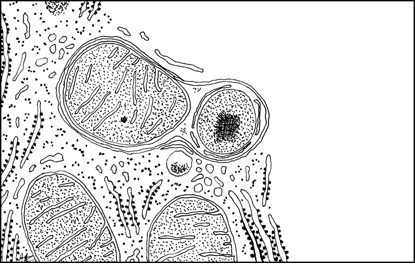 |
| Autophagosome renfermant une mitochondrie et un peroxysome. Les mitochondries ont une durée de vie qui est d’une dizaine de jours, en moyenne. |
Les lysosomes sont aussi alimentés en substrats à dégrader par les autophagosomes. L’autophagie est un mécanisme d’autodestruction contrôlée de portions de la cellule ; il fut découvert en 1962 par Thomas P. Ashford, un étudiant du laboratoire de Keith Porter (The Rockefeller Institute for Medical Research, New York), en observant les hépatocytes d’animaux ayant reçu une injection de glucagon. Porter pensait être en présence du mécanisme de formation des lysosomes.
Référence : Ashford TP, Porter KR Cytoplasmic Components in Hepatic Cell Lysosomes (1962)
L’autophagie se déroule par étapes : elle débute par l’apparition d’une membrane en forme de croissant. Les données de la cryo-tomographie électronique suggèrent que cette membrane est issue du reticulum endoplasmique : elles montrent des connexions entre les membranes des vacuoles autophagiques et des citernes du reticulum. Cette membrane, dénommée « phagophore », entre dans une phase d’élongation, séquestre une partie du cytoplasme et donne naissance à une vésicule à double membrane – l’autophagosome – contenant du matériel à dégrader. La vacuole autophagique fusionne avec un lysosome donnant naissance à un autolysosome. Les hydrolases lysosomales dégradent le contenu (protéines malformées, organites endommagés ou en fin de vie) ainsi que la membrane interne de l’autophagosome ; les micromolécules libérées sont utilisées par la cellule. Christian de Duve, dans le laboratoire duquel les lysosomes ont été découverts, proposa le terme « autophagie » pour décrire un phénomène observé par plusieurs auteurs dans les cellules hépatiques et rénales.
A la différence de la phagocytose, qui est essentiellement un mécanisme de défense des cellules contre les infections et l’invasion par des bactéries, l’autophagie est un mécanisme de maintenance et de survie par lequel les cellules dégradent et recyclent une partie de leur propre substance. L’autophagie intervient dans des phénomènes essentiels : (i) le renouvellement des organites subcellulaires : dans des conditions de nutrition normales, la majeure partie des composants d’un hépatocyte est renouvelée chaque semaine ; l’autophagie est le pivot de l’homéostasie cellulaire ; (ii) l’autodestruction contrôlée de certains tissus ; (iii) l’involution de certains organes comme le rein ; au cours de l’embryogenèse, le tissu rénal est partiellement détruit puis reconstruit pour former le rein mature. Enfin, l’autophagie est aussi un mécanisme de survie des cellules en souffrance, par exemple par dénutrition : après un jeûne prolongé, les cellules consomment leurs propres constituants.
Les travaux du groupe de Per O. Seglen (Electron Microscopical Unit for Biological Sciences, Institute of Biology, University of Oslo) constituent la première tentative d’élucidation du mécanisme de l’autophagie ; elle est essentiellement basée sur l’observation au microscope électronique de coupes ultrafines de cellules hépatiques isolées. C’est Seglen qui a découvert le pré-autophagosome et qui l’a dénommé « phagophore ». Comme il est dit plus haut, en s’allongeant et en englobant le matériel cytoplasmique la membrane en forme de croissant devient la vacuole autophagique initiale : l’autophagosome. Seglen découvrit aussi un inhibiteur spécifique de l’autophagie : une adénine substituée par un groupe méthyle en position N3, la 3-méthyladénine ; lorsque les cellules de foie de rat sont mises en contact avec ce métabolite, l’examen au microscope électronique révèle l’absence d’autophagosomes dans leur cytoplasme ; ce métabolite bloque leur formation.
Référence : Seglen PO, Gordon PB 3-Methyladenine: specific inhibitor of autophagic/lysosomal protein degradation in isolated rat hepatocytes (1982)
Dans la suite de leurs travaux, les collaborateurs de Seglen identifièrent deux molécules qui provoquent une accumulation d’autophagosomes dans le cytoplasme : l’acide aminé asparagine et la vinblastine, l’inhibiteur des microtubules du cytosquelette. Ces deux agents sont des perturbateurs du trafic intracellulaire entre vacuoles autophagiques, endosomes et lysosomes ; avec la 3-méthyladénine, ils constituent des outils essentiels pour démêler le mécanisme de l’autophagie. La 3-méthyladénine inhibe la phosphatidylinositol 3-kinase de classe III, qui catalyse la formation de phosphatidylinositol-3-phosphate, un phospholipide membranaire présent dans le système endosomal ; il joue un rôle clé dans le tri des protéines dans les endosomes et dans les premières étapes de la formation de l’autophagosome. En suivant, dans les hépatocytes isolés, le sort du [14C]-lactose séquestré dans les vacuoles autophagiques et celui de la beta-galactosidase dans des vésicules d’endocytose, Paul B. Gordon et Per O. Seglen (Institute for Cancer Research, Oslo University Hospital) ont montré que l’asparagine empêchait la fusion entre ces deux structures avant l’intervention des lysosomes. Ils ont ainsi définit un nouveau compartiment fonctionnel pré lysosomal commun aux voies autophagique et endocytaire, qu’ils ont dénommé « amphisome ».
Référence : Gordon PB, Seglen PO Prelysosomal convergence of autophagic and endocytic pathways (1988)
Monica Fengsrud et ses collègues firent preuve de beaucoup d’ingéniosité technique dans la mise au point d’une approche leur permettant de suivre au microscope l’évolution des différents organites au cours de l’autophagie. Pour évaluer la dégradation dans les vacuoles autophagiques, ils mesuraient le rapport entre la dégradation par les hydrolases lysosomales de deux enzymes cytosoliques : la superoxyde dismutase à cuivre-zinc (résistante à la dégradation) et l’anhydrase carbonique anhydrase (très sensible à la dégradation). Pour distinguer les lysosomes des endosomes ils ont utilisé la glycoprotéine membranaire lgp120 (Lysosomal GlycoProtein 120, LAMP1, Lysosome-Associated Membrane Protein 1), absente dans les endosomes précoces. L’endocytose dans les vacuoles autophagiques fut détectée par la capture de sérum albumine de bœuf marquée à l’or colloïdal. Les résultats ont révélé la convergence, dans les hépatocytes de rat, entre autophagie et endocytose, deux phénomènes impliquant les lysosomes. Les voies autophagiques et endocytaire se rejoignent au point de fusion entre autophagosome et endosomes tardifs : les amphisomes.
Références : Seglen PO, Gordon PB 3-Methyladenine: specific inhibitor of autophagic/lysosomal protein degradation in isolated rat hepatocytes (1982)
Fengsrud M, Roos N, Berg T, Liou W, Slot JW, Seglen PO Ultrastructural and Immunocytochemical Characterization of Autophagic Vacuoles in Isolated Hepatocytes: Effects of Vinblastine and Asparagine on Vacuole Distributions (1995)
Si Per O. Seglen a abordé l’étude de l’autophagie par une approche biochimique, dix ans plus tard, Yoshinori Ohsumi et ses collaborateurs, Noboru Mizushima et Tamotsu Yoshimori (National Institute for Basic Biology, Okazaki) ont utilisé l’approche génétique pour étudier les mécanismes moléculaires de la macroautophagie chez la levure Saccharomyces cerevisiae. Ils commencèrent par démontrer que l’autophagie existe chez les levures en les soumettant à une carence en azote. En 1992, furent publiés les résultats sur l’identification des premiers gènes APG (AutoPhagGy).
Références : Takeshige K, Baba M, Tsuboi S, Noda T, Ohsumi Y Autophagy in yeast demonstrated with proteinase-deficient mutants and conditions for its induction (1992)
Tsukada M, Ohsumi Y Isolation and characterization of autophagy-defective mutants of Saccharomyces cerevisiae (1993)
En 1994, d’autres gènes furent découverts : les gènes AUT (autophagy), par Michael Thumm et coll. (Institut für Biochemie, Universität Stuttgart) et les gènes CVT (Cytoplasm to Vacuole Targeting), par le groupe de Daniel J. Klionsky (Life Sciences Institute, University of Michigan) ; des travaux ultérieurs montrèrent que ce sont des gènes ATG. Pour éviter la multiplication des appellations, la nomenclature « ATG » fut introduite en 2003 à l’initiative de Klionsky. Au total, ce sont 15 gènes qui sont impliqués dans le processus autophagique chez les levures. L’intervention des protéines ATG dans la formation de l’autophagosome est séquentielle : les systèmes de conjugaison ATG12-ATG5 et ATG8-phosphatidyléthanolamine sont nécessaires pour l’élongation de la membrane pré-autophagosomale, avant la formation de l’autophagosome. À la fin des années 1990, Mizushima, puis Beth Levine et Guido Kroener (Howard Hughes Medical Institute, University of Texas Southwestern Medical Center), montrèrent que des gènes ATG sont conservés chez les mammifères. Yoshinori Ohsumi reçut le prix Nobel de physiologie ou médecine 2016.
Références : Thumm M, Egner R, Koch B, Schlumpberger M, Straub M, Veenhuis M, Wolf DH Isolation of autophagocytosis mutants of Saccharomyces cerevisiae (1994)
Harding TM, Morano KA, Scott SV, Klionsky DJ Isolation and characterization of yeast mutants in the cytoplasm to vacuole protein targeting pathway (1995)
Mizushima N, Noda T, Yoshimori T, Tanaka Y, Ishii T, George MD, Klionsky DJ, Ohsumi M, Ohsumi Y A protein conjugation system essential for autophagy (1998)
Klionsky DJ, Cregg JM, Dunn WA Jr, Emr SD, Sakai Y, Sandoval IV, Sibirny A, Subramani S, Thumm M, Veenhuis M, Ohsumi Y A unified nomenclature for yeast autophagy-related genes (2003)
Levine B, Kroemer G Autophagy in the pathogenesis of disease (2008)
L’autophagie est un mécanisme de dégradation non sélectif d’importance vitale ; dans certains cas, le recrutement du matériel à dégrader (organites, agrégats protéiques) est un mécanisme sélectif mettant en jeu la protéine LC3 (Light Chain 3), associée à la membrane de la vacuole autophagique ou, chez la levure, la protéine ATG8 qui intervient dans l’élongation et la fermeture de l’autophagosome. Dès la fécondation de l’ovule, les mitochondries maternelles sont éliminées de l’œuf par autophagie. Ensuite, l’autophagie assure l’homéostasie des tissus et des organes ; sa stimulation ralentit le vieillissement chez la levure et chez les mammifères.
Article de revue : Mizushima N, Komatsu M Autophagy: Renovation of Cells and Tissues (2011)
A la fin de ce sous-chapitre, je voudrais faire mention du rôle joué par les lysosomes dans la production de peptides antigéniques. Les lymphocytes T CD4 (lymphocytes T auxiliaires, helper) sont des acteurs majeurs de la réponse immunitaire. Ils reconnaissent les peptides antigéniques présentés par des molécules d’histocompatibilité de classe II – chez l’homme HLA-DR, DP, DQ – à la surface des cellules présentatrices d’antigènes (macrophages, cellules dendritiques, lymphocytes B activés). Les lymphocytes T CD4 agissent en activant d’autres cellules du système immunitaire : ils dirigent les lymphocytes B dans leur différenciation vers la production d’anticorps.
Les molécules du complexe majeur d’histocompatibilité II sont des glycoprotéines dimériques, dotées d’un peptide signal amino-terminal ; elles sont synthétisées dans le domaine ribosomal du reticulum endoplasmique, où elles s’associent à une protéine membranaire de type 2, la chaîne invariante ; la fonction de cette chaperonne est double : (i) protéger les sites de fixation des peptides contre toute association prématurée avec des peptides (ii) accompagner le complexe au cours des étapes de glycosylation dans le reticulum endoplasmique et le Golgi. Doté d’un second signal topogénique, le signal mannose 6-phosphate, le complexe atteint le réseau trans-golgien, d’où il est dirigé vers les endosomes. A pH acide, les protéases endosomales dégradent la chaîne invariante laissant un peptide (class II associated invariant chain peptide, CLIP) associé à la fente des chaînes α et β. Les peptides reconnus par les lymphocytes T auxiliaires sont présents dans le compartiment endosomes – lysosomes. Ils ont été générés à partir d’antigènes endocytés – ou phagocytés – par les cellules présentatrices et dégradés par les protéases à pH acide. C’est dans ce compartiment que les molécules du complexe majeur d’histocompatibilité II rencontrent les peptides antigéniques et que se fait l’échange CIP – peptide.
Note : Pour la rédaction de ce paragraphe, les informations m’ont été fournies par le Dr. Pierre Coulie (de Duve Institute, Bruxelles), qui en a aussi supervisé le texte.
Fonctions des Lysosomes
| Renouvellement (turn over) des constituants et des protéines intra- et extra-cellulaires |
|---|
| Dégradation et recyclage des organites cellulaires |
| Maintien de l’homéostasie cellulaire |
| Contrôle de qualité des protéines |
| Dégradation des protéines mal formées ou anormales |
| Dégradation des récepteurs non recyclés de la membrane plasmique |
| Réparation des membranes cellulaires |
| Fusion des lysosomes avec la membrane endommagée |
| Invagination de la membrane et endocytose du site de la lésion |
| Homéostasie du cholestérol et maintien de l’intégrité de la membrane plasmique |
| Endocytose des lipoprotéines (LDL) plasmatiques |
| Transfert vers la membrane plasmique du cholestérol libéré dans les lysosomes |
| Remodelage du squelette osseux |
| Hydrolyse de protéines de la matrice extracellulaire osseuse par les ostéoclastes |
| (Cathepsine K, phosphatase acide pourpre) |
| Maturation des pro-hormones |
| (production de thyroxine dans la lumière des follicules thyroïdiens par protéolyse extracellulaire de la thyroglobuline par la cathepsine K) |
| Digestion des bactéries et autres agents pathogènes par les hydrolases lysosomiales dans les phagosomes des macrophages |
| Production de peptides antigéniques reconnus par des lymphocytes T |
| Voie de présentation par les molécules du Complexe majeur d’histocompatibilité de classe II |
| Régulation de la sécrétion des cellules hématopoïétiques |
| (stockage dans les lysosomes des produits de sécrétion) |
Clairance cellulaire
Les résultats des travaux d’Andrea Ballabio et de ses associés (Telethon Institute of Genetic and Medicine, Università di Napoli Federico II) ont transformé la conception que l’on avait du rôle des lysosomes dans la dégradation et le recyclage des déchets ; leur fonction dans la clairance cellulaire est un processus dynamique soumis à un contrôle et à une étroite régulation.
Marco Sardiello et coll. ont découvert que la biogenèse et la fonction des lysosomes sont soumises à un programme génétique ; le réseau CLEAR (Coordinated Lysosomal Expression and Regulation) rassemble des gènes impliqués dans la synthèse de plusieurs enzymes lysosomaux. L’expression des gènes du réseau CLEAR est régulée au niveau de la transcription par le facteur TFEB (Transcription Factor EB) de la sous famille des facteurs de transcription à motif hélice – boucle – hélice et tirette à leucines bHLH (basic Helix-Loop-Helix). TFEB est localisé dans le cytoplasme des cellules ; dans des conditions de surcharge lysosomale, de stress ou de jeûne, il se fixe sous forme de dimère (par les domaines bHLH) sur un promoteur commun à de nombreux gènes codant pour les enzymes lysosomaux : l’élément CLEAR (Coordinated Lysosomal Expression and Regulation element), une séquence palindromique de dix paires de bases :
-G-T-C-A-C-G-T-G-A-C-
-C-A-G-T-G-C-A-C-T-G-
Référence : Sardiello M, Palmieri M, di Ronza A, Medina DL, Valenza M, Gennarino VA, Di Malta C, Donaudy F, Embrione V, Polischuk RS, Banfi S, Parenti G, Cattaneo E, Ballabio A A gene network regulating lysosomal biogenesis and function (2009)
Carmine Settembre et coll. montrèrent que le facteur de transcription EB contrôle aussi l’autophagie. L’activité de TFEB est régulée par un processus de phosphorylation (forme inactive) – dé-phosphorylation (forme active). Sous forme phosphorylé sur une sérine par une sérine/thréonine kinase membranaire, la kinase mTOR (Mammalian Target Of Rapamycin), TEFB est localisé dans le cytoplasme des cellules. La kinase mTOR appartient au système protéique membranaire LYNUS (LYsosome NUtrient Sensing machinery) capable d’estimer le niveau des réserves de la cellule en nutriments. En cas de jeûne, mais aussi de stress, ou d’accumulation des déchets, la kinase mTOR est désactivée et TFEB est dé-phosphorylé par la calcitonine, activée par les ions Ca2+. Le facteur de transcription subit alors une translocation dans le noyau où il déclenche l’expression coordonnée des gènes codant pour les enzymes et les protéines membranaires (V-ATPases, Na ATPase) des lysosomes, et pour les protéines impliquées dans l’autophagie.
L’autophagie est un processus au cours duquel une partie des protéines cellulaires sont dégradées ; elle débute par la ségrégation d’une portion du cytoplasme et des organites qui s’y trouvent à l’intérieur d’une double-membrane ; la fusion de cet auto-phagosome avec des lysosomes aboutit à la dégradation de son contenu : organites endommagés ou agrégats protéiques toxiques. Ce processus permet la survie en période de jeûne ; il est également activé au cours de la transformation d’une cellule souche en une cellule différenciée fonctionnelle. Dans les cellules où TFEB est surexprimé, on observe une augmentation du nombre de lysosomes et une dégradation des déchets accrue (régulation positive).
Références : Settembre C, Di Malta C, Polito VA, Arencibia MG, Vetrini F, Erdin S, Erdin SU, Huynh T, Medina D, Colella P, Sardiello M, Rubinsztein D, Ballabio A TFEB links autophagy to lysosomal biogenesis (2011)
Medina DL, Fraldi A, Bouche V, Annunziata F, Mansueto G, Spampanato C, Puri C, Pignata A, Martina JA, Sardiello M, Palmieri M, Polishchuk R, Puertollano R, Ballabio A Transcriptional Activation of Lysosomal Exocytosis Promotes Cellular Clearance (2011)
Settembre C A lysosome-to-nucleus signalling mechanism senses and regulates the lysosome via mTOR and TFEB (2012)
Medina DL Lysosomal calcium signals control autophagy through calcineurin and TFEB (2015)
Les lysosomes de certaines cellules pratiquent une forme de digestion extracellulaire ; les lysosomes fusionnent avec la membrane plasmique et déversent leur contenu à l’extérieur de la cellule. L’exocytose lysosomale est un processus soumis à une régulation ; il se déroule en deux étapes : (i) le facteur de transcription EB stimule le recrutement des lysosomes à proximité de la membrane plasmique ; (ii) TFEB active le canal à Ca2+ MCOLN1 (MuCOLipiN) de la membrane des lysosomes et des endosomes ; l’augmentation de la concentration intracellulaire en Ca2+ provoque la fusion entre elles des membranes lysosomale et plasmique. Les ostéoclastes et les chondroclastes sont des macrophages qui participent au remodelage et au renouvellement du tissu osseux en exportant dans le milieu extracellulaire des hydrolases lysosomales et un suc acide qui dégradent les matrices osseuse et cartilagineuse. Le suc acide dissout l’hydroxyapatite, une combinaison de phosphate et d’hydroxyde de calcium, qui constitue la partie minérale de l’os. L’échafaudage de collagène est attaqué par les enzymes. Les fragments sont intériorisés dans les ostéoclastes et digérés dans les lysosomes. Les matrices osseuse et cartilagineuse sont ensuite reconstruites par les ostéoblastes et les chondroblastes.
Dans la thyroïde, les lysosomes interviennent dans la sécrétion hormonale. La thyroglobuline synthétisée dans les cellules de l’épithélium thyroïdien est sécrétée dans les follicules thyroïdiens où elle subit une iodination. Elle est intériorisée par endocytose dans les cellules épithéliales. Les endosomes fusionnent avec les lysosomes où la thyroglobuline est dégradée avec libération de thyroxine. Les cellules épithéliales libèrent l’hormone thyroïdienne dans la circulation sanguine.
Références : Jaiswal JK, Andrews NW, Simon SM Membrane proximal lysosomes are the major vesicles responsible for calcium-dependent exocytosis in nonsecretory cells (2002)
Tucker WC, Weber T, Chapman ER Reconstitution of Ca2+-regulated membrane fusion by synaptotagmin and SNAREs (2004)
Article de revue : Andrews NW Regulated secretion of conventional lysosomes (2000)
Pathologie des lysosomes (Lysosomal storage disorders)
Maladies neurodégénératives
En 1929, Edgar von Gierke (Pathologisches Bacteriologisches Institut, Städtiches Klinikum Karlsruhe) publia dans Beiträge zur Pathologischen Anatomie und zur Allgemeinen Pathologie ses observations sur la « maladie de thésaurisation du glycogène » observée chez deux enfants présentant une hypertrophie du foie et des reins ; le glycogène présent dans ces organes était anormalement résistant à l’hydrolyse. La maladie de von Gierke porte aujourd’hui le nom de glycogénose de type I. Les premiers cas cliniques de glycogénose de type II (Glycogen storage disease type 2, Acid maltase deficiency) furent décrits par Johan C. Pompe aux Pays-Bas et par W. Putschar et G. Bishoff en Allemagne. Pompe découvrit, dans le cœur d’abord mais aussi dans tous les tissus qu’il examina, une accumulation de glycogène, révélée par la coloration au Carmin de Best. Cette forme de pathologie atteignant principalement le cœur, amena Pompe, Putschar et Bishoff à penser qu’il s’agissait sans doute d’une maladie différente de la maladie de von Gierke. Pompe fit de cette affection grave entrainant le décès du patient – désormais appelée « Maladie de Pompe » – l’objet de sa thèse.
Références : Von Gierke E Glykogenspeicherkrankheit der Leber und Nieren (1929)
Pompe JC Over idiopathische hypertrophie van het hart (1932)
Putschar W Uber angeborne Glycogenspeicherkrankheit des herzens:Thesaurismosis glycogenica (v.Gierke) (1932)
Bischoff G Zum klinischen Bild der Glykogen-Speicherungskrankheit (Glykogenose) (1932)
Pompe JC Cardiomegalia Glycogenica (1936)
Au début des années 1950, Gerty Theresa Cori (Washington University, Saint Louis, prix Nobel de physiologie ou médecine 1947) apporta une contribution essentielle à la connaissance des glycogénoses (Glycogen storage diseases) en mettant en lumière la cause de l’accumulation anormale de glycogène dans les tissus. Dans les cas étudiés, elle mit en évidence l’absence ou la déficience d’un enzyme de la voie de dégradation du glycogène : (i) la glucose-6-phosphatase dans la Maladie de von Gierke (Glycogen storage disease I) ; (ii) l’enzyme débranchant du glycogène (Glycogen debranching enzyme) dans la Maladie de Cori-Forbes (Glycogen storage disease III) ; la glycogénose de type III porte son nom. Gerty Cori fut la première à démontrer qu’une carence enzymatique est à l’origine d’une maladie génétique humaine.
Article de revue : Cori GT Glycogen structure and enzyme deficiencies in glycogen storage disease (1954)
Henri-Géry Hers (Laboratoire de Chimie physiologique, Université catholique de Louvain) montra que dans de la maladie de Pompe la déficience porte sur un enzyme qui, dans les conditions habituelles, joue un rôle tout à fait secondaire dans le catabolisme du glycogène : l’α-1,4-glucosidase hydrolyse à pH 5 des polysaccharides, des oligosaccharides et des disaccharides comme le maltose, d’où son nom de « maltase acide » et l’appellation « Déficience en maltase acide » donnée à la maladie de Pompe. Hers avait précédemment découvert un nouveau type de glycogénose causée par un déficit en phosphorylase, l’enzyme qui dégrade le glycogène en glucose-1-phosphate ; la glycogénose de type VI porte le nom de maladie de Hers.
Références : Hers HG α-Glucosidase deficiency in generalized glycogen-storage disease (Pompe’s disease) (1963)
Hers HG Étude enzymatique des glycogénoses (1959)
Le fait que la maltase ait un pic d’activité à pH acide attira l’attention des chercheurs du Groupe de Louvain, où Christian de Duve et coll. venaient de découvrir les lysosomes : le résultat du fractionnement par centrifugation d’homogénat de foie montra que la distribution de la maltase dans les fractions est superposable à celle de la phosphatase acide. L’examen au microscope électronique de biopsies provenant d’un jeune patient atteint de la maladie de Pompe révéla la présence dans les cellules hépatiques de lysosomes gorgés de rosettes de glycogène. La présence d’α-1,4-glucosidase dans les lysosomes révéla l’existence de deux voies métaboliques de dégradation du glycogène en glucose : une voie « normale » passant par la glycogène phosphorylase cytosolique, et une voie passant par l’autophagie. Lorsque le glycogène s’accumule dans le cytosol, il est séquestré dans des vacuoles et dégradé par la maltase acide des lysosomes. A l’issue de son travail sur la glycogénose de type II, Hers formula l’hypothèse que d’autres pathologies de stockage, comme la Maladie de Gaucher ou la Maladie de Tay-Sachs, pourraient avoir pour cause un déficit en enzymes lysosomaux.
Référence : Hers HG The role of lysosomes in the pathogeny of storage diseases (1972)
La maladie de Pompe est ainsi devenue la première maladie de surcharge lysosomale identifiée. Elle s’inscrit dans le cadre général des erreurs innées du métabolisme (Inborn error of metabolism) découvertes par Archibald Garrod. Ce sont des maladies génétiques rares de surcharge des lysosomes dans lesquelles la mutation d’un gène entraîne l’absence ou le dysfonctionnement d’une hydrolase acide, les déchets non digérés s’accumulent, ce qui entraîne le dysfonctionnement de la cellule, puis de l’organe ou de plusieurs organes. On a identifié de 50 à 70 thésaurismoses lysosomales dont la gravité témoigne s’il en était besoin de l’importance du rôle des lysosomes dans la clairance cellulaire, le recyclage et l’élimination des déchets. On peut tenter de classer les thésaurismoses de manière plus ou moins arbitraire selon le type de surcharge ; c’est ainsi que l’on distingue : (i) Maladie de Gaucher (déficit en glucocérébrosidase), Maladie de Niemann-Pick (sphingomyélinase), Maladie de Fabry (alpha-glucosidase A) ; (ii) Syndrome de Hurler (alpha-L-iduronidase), Syndrome de Hunter (iduronate-2-sulfatase), Maladie de Sanfilippo A (déficit en héparane sulfamidase) ; (iii) Alpha-mannosidose, Glycogénose de type II. Les thésaurismoses sont des maladies héréditaires le plus souvent autosomiques récessives ; les deux parents doivent être porteurs du gène muté ; seules la maladie de Fabry et le Syndrome de Hunter sont des pathologies liées à l’X.
Deux approches sont parallèlement suivies pour traiter les patients atteints de thésaurismoses : (i) la thérapie enzymatique substitutive, qui consiste à administrer par perfusion au patient l’enzyme manquant, a été essayée dans la Maladie de Sanfilippo A (déficit en héparane sulfamidase), la Maladie de Gaucher, la Maladie de Fabry, dans la Leucodystrophie métachromatique (déficit en arylsulfatase A) et dans des mucopolysaccharidoses. (ii) la stimulation de la clairance des déchets accumulés ; un grand espoir est suscité par cette stratégie mise en œuvre dans le groupe d’Andrea Ballabio (Telethon Institute of Genetics and Medicine, Napoli). Je renvoie le lecteur au sous-chapitre « Clairance cellulaire » où je décris la découverte du facteur de transcription TFEB (Transcription Factor EB) ; en se fixant sur les sites E-box de leur promoteur, TFEB contrôle la transcription des gènes CLEAR (Coordinated Lysosomal Enhancement And Regulation) impliqués dans la biogenèse et l’activité des lysosomes. Dans les cellules où TFEB est surexprimé, on observe une augmentation du nombre de lysosomes, de l’activité des enzymes lysosomaux (régulation positive), de l’autophagie et de l’exocytose. La capacité des cellules à digérer les déchets, et à expulser leurs produits de dégradation est fortement augmentée. Cette stratégie a été appliquée avec succès dans la Maladie de Batten (céroïde-lipofuscinose) ou dans des Mucopolysaccharidoses. Cette approche thérapeutique n’est pas seulement applicable aux maladies rares que sont les thésaurismoses ; les maladies neuro-dégénératives avec accumulation de dépôts intracellulaires d’agrégats de protéine bêta-amyloïde et de protéine tau (maladie d’Alzheimer) ou de protéines anormales comme l’α-synucléine (Maladie de Parkinson) pourraient en bénéficier.
Note : Pour la rédaction de ce sous-chapitre, j’ai tenu compte des remarques formulées et des corrections proposées par le Dr Émile Van Schaftingen, qui fut un proche collaborateur d’Henri-Géry Hers.
Thérapie lysosomotrope
Les protozoaires flagellés Leishmania transmettent à l’homme des infections graves, voire mortelles. Leishmania donovani infecte les macrophages du foie, de la rate et de la moelle osseuse en passant par le système phagosomes – lysosomes. D’autres protozoaires, responsables d’affections parasitaires, passent aussi par le système vacuolaire et par les phagosomes – lysosomes : Toxoplasma gondii (toxoplasmose), coccidies (coccidiose), Trypanosoma cruzi (maladie de Chagas), Plasmodium (malaria). Une thérapie lysosomotrope fut envisagée pour combattre ces parasitoses ; elle consiste à faire pénétrer par endocytose dans les cellules infectées des drogues anti-parasitaires couplées à des vecteurs macromoléculaires,; après hydrolyse du vecteur, ou de la liaison vecteur-drogue par les enzymes lysosomiaux, la substance anti-parasitaire est libérée dans un espace confiné, en contact avec le parasite.
Références : De Duve C, Trouet A Lysosomes and lysosomotropic drugs in host-parasitic relationship (1973)
Jadin JM, Trouet A, Van Hoof F, Bioul-Marchand M, Maldague P, Jadin-Nyssens M Étude comparative d’une chimiothérapie lysosomotrope dans la maladie de Chagas et dans le Nagana (1977)
Partant du même principe, André Trouet et Christian de Duve (Laboratoire de Chimie physiologique, Université Catholique de Louvain) imaginèrent une thérapie lysosomotrope pour traiter certaines formes de cancers. De nombreuses substances antinéoplasiques utilisées en thérapie anti-tumorale sont aussi des cytostatiques ; elles bloquent l’activité proliférative des cellules cancéreuses, c’est-à-dire leur capacité à se diviser. Les antinéoplasiques manquent de spécificité ; les cellules germinales, les cellules souches des globules blancs et des globules rouges et d’une manière plus générale les cellules des tissus à taux de renouvellement élevé – sang, peau, muqueuses -, sont aussi des cibles. De plus, pour un certain nombre d’agents anti-tumoraux, la différence entre dose thérapeutique et dose toxique est faible. Dans les années 1960-1970, on était en quête d’une thérapie anti-tumorale efficace et spécifique, ciblant les cellules tumorales à l’exclusion des cellules saines. A côté de la recherche de nouveaux agents par extraction et criblage à partir de matériels divers – une approche longue et coûteuse -, et de perspectives thérapeutiques nouvelles résultant d’une meilleure connaissance des mécanismes moléculaires et cellulaires de la cancérisation, s’ouvrait l’option de modifier la structure des antinéoplasiques existants pour les rendre moins toxiques et plus efficaces, par exemple par couplage à des macromolécules.
Références : de Duve C, de Barsy T, Poole B, Trouet A, Tulkens P, Van Hoof F Lysosomotropic agents (1974)
Trouet A, Deprez-de Campeneere D, Maldague P, Jadin JM, Van Hoof F The Concept of Lysosomotropic Chemotherapy: Applications to Neoplastic and Parasitic Diseases (1977)
Trouet A Carriers for drugs (1977)
La « thérapie lysosomotrope » imaginée par Trouet et de Duve est essentiellement basée sur l’idée que l’endocytose est plus élevée chez les cellules tumorales que chez les cellules dites normales. Vers le milieu des années 1950, la croyance s’est imposée que les besoins en protéines des cellules tumorales dépassent leur capacité à les synthétiser ; pour compenser le déficit, les cellules tumorales à croissance rapide sont des « pièges à azote » qui captent, par pinocytose, des protéines dans le milieu extracellulaire et le plasma. Un certain nombre de résultats font état d’un taux de captation des protéines par pinocytose élevé dans les cellules de tumeurs expérimentales ou humaines : leucémie, lymphome, réticulosarcome, hépatome, glioblastome ; je cite quelques articles sur le sujet :
Références : Cohen S, Beiser SM, Hsu KC Immunohistochemical study of the uptake of serum proteins by neoplastic liver cells (1961)
Ghose T, Nairn RC, Fothergill JE Uptake of proteins by malignant cells (1962)
Easty GC, Yarnell MM, Andrews RD The uptake of proteins by normal and tumour cells in vitro (1964)
Ioverno L, Levis A, Palumbo A, Ghezzo F, Genetta C, Pegoraro L Phagocytic activity and cytochemical characterization of acute human myeloblastic leukemia cells (1982)
Voir aussi : Anderson D, Bush H, Greene HS, Simbonis S Studies on the metabolism of plasma proteins in tumor-bearing rats. II. Labeling of intracellular particulates of tissues by radioactive albumin and globulin (1956)
Henderson JF, LePage GA The Nutrition of Tumors: A Review (1959)
Lepage GA, Henderson JF Biochemistry of tumors (1960)
Busch H, Fujiwara E, Firszt DC Studies on the metabolism of radioactive albumin in tumor-bearing rats (1961)
En théorie, le ciblage d’une substance chimiothérapique nécessite qu’elle soit liée à un ligand reconnu par un récepteur spécifique des cellules tumorales. La mise au point pratique d’une telle stratégie représente un travail de très longue haleine. L’approche choisie par Trouet, basée sur la différence d’activité endocytaire entre cellules normales et cancéreuses, vise à court-circuiter ce laborieux processus. Elle est plus rapide, mais présente le défaut d’être quantitative et non qualitative comme dans le modèle ligand-récepteur spécifique. Le vecteur macromoléculaire sélectionné fut l’ADN et l’antinéoplasique, les anthracyclines daunomycine (daunorubicine) ou adriamycine (doxorubicine, un inhibiteur de la topo-isomérase II). La daunomycine pénètre dans les cellules par diffusion. Son emploi est limité par sa toxicité : injectée par voie intramusculaire elle provoque des nécroses musculaires, notamment du muscle cardiaque. La formation du complexe ADN-daunorubicine se fait par contact entre les deux ingrédients dans des conditions définies ; la daunorubicine s’intercale dans le petit sillon de l’ADN. Un certain nombre de conditions doivent être remplies : (i) le complexe doit être stable dans le sang et les milieux intracellulaires ; (ii) le complexe doit pénétrer dans les cellules par endocytose ou pinocytose ; on a pu le montrer sur des cellules L1210 en culture ; (iii) après passage des endosomes aux lysosomes, l’association vecteur – agent anti-tumoral doit être dissociable, libérant ainsi le principe actif ; le vecteur ADN est digéré par les DNAses lysosomiales ; (iv) après hydrolyse du vecteur, l’agent thérapeutique libéré doit être résistant à la digestion par le vaste éventail des enzymes hydrolytiques des lysosomes.
Dans l’espace réduit des lysosomes, les anthracyclines atteignent des concentrations élevées et fragilisent la membrane lysosomiale, ce qui entraîne une libération de cathepsines dans le cytoplasme. On contourne ainsi un obstacle majeur auquel se heurte la chimiothérapie classique : en activant la mort cellulaire par rupture des lysosomes, on compense le blocage de la voie classique de l’apoptose chez les cellules tumorales. Des essais thérapeutiques furent entrepris, d’abord sur des cellules L1210 en culture, puis sur la forme intrapéritonéale de la leucémie L1210 chez la souris DBA/2 (Dilute Brown Non-Agouti) et enfin chez des patients. Après des débuts encourageants et quelques succès initiaux, les essais en clinique humaine durent être abandonnés. La liaison ADN-daunorubycine n’est pas aussi stable dans le plasma sanguin qu’on le croyait, ce qui explique peut-être pourquoi des chercheurs du National Cancer Institute (Bethesda), intéressés par le ciblage (targeting) de substances anti-tumorales, ne sont pas parvenus pas à reproduire les résultats de Trouet et de Duve. D’autre part, l’injection d’ADN a des patients n’est pas sans soulever de multiples problèmes, notamment sur le plan éthique. C’est pourquoi la daunorubicine a été ultérieurement conjuguée à la sérum albumine par une liaison amide entre le groupe aminé de l’anthracycline et un groupe carboxyle de la protéine. L’intercalation d’un espaceur de trois acides aminés entre la protéine et la drogue augmente la sensibilité à l’hydrolyse dans les lysosomes.
Références : Deprez-de Campeneere D, Trouet A DNA-anthracycline complexes. I. Toxicity in mice and chemotherapeutic activity against L1210 leukemia of daunorubicin-DNA and Adriamycin-DNA (1965)
Trouet A, Deprez-De Campeneere D, de Duve C Chemotherapy through Lysosomes with a DNA-Daunorubycin Complex (1972)
Langslet A, Oye I, Lie SO Decreased cardiac toxicity of Adriamycin and daunorubicin when bound to DNA (1974)
Cornu G, Michaux JL, Sokal G, Trouet A Daunorubicin-DNA : Further Clinical Trials in acute non-lymphoblastic leukemia (1974)
Trouet A, de Duve C, De Smet-Malengreaux M, Atassi G Experimental leukemia chemotherapy with a « lysosomotropic » adriamycin-DNA complex (1974)
Trouet A, Sokal G Clinical Studies with Daunorubicin-DNA Complexes: A Review (1974)
Longueville J, Maisin H Combined Therapy with Adriamycin-DNA, Vincristine and Medoxy-Progesterone Acetate in Metastatic Breast Cancer (1975)
Michaux JL, Cornu G, Sokal G, Trouet A Preliminary clinical trials with the adriamycin-DNA complex in human leukemias and non-Hodgkin lymphomas (1975)
Deprez-De Campeneere D, Baurain R, Huybrechts M, Trouet A A Comparative study in mice of the toxicity, pharmacology, and therapeutic activity of daunorubicin-DNA and doxorubicin-DNA complexes (1979)
Trouet A, Masquelier M, Baurain R, Deprez-De Campeneere D A covalent linkage between daunorubicin and proteins that is stable in serum and reversible by lysosomal hydrolases, as required for a lysosomotropic drug-carrier conjugate: in vitro and in vivo studies (1982)
Note. L’implication des lysosomes dans une thérapie anti-tumorale continue à faire l’objet de recherches. Je cite comme exemple les travaux de Teodora Krol et de Wojciech et Ewa Trybus (Jan Kochanowski University, Kielce) :
Trybus W, Trybus E, Krol T Lysosomes as a Target of Anticancer Therapy (2023)